전자는 파동처럼 행동한다
물리학자들은 빛이 전자기파라는 사실을 오랫동안 알고 있었습니다. 오늘날까지 빛은 파동 행동의 모든 징후를 명확하게 보여주기 때문에 아무도 이 위치를 의심하지 않습니다.
오리처럼 걷고, 오리처럼 헤엄치고, 오리처럼 꽥꽥거리는 새를 보면 우리는 그 새를 오리라고 부른다. 그래서 빛은 전자기파빛에서 그러한 파동의 행동에 대한 객관적으로 관찰된 징후를 기반으로 합니다.

그러나 19세기 후반과 20세기에 물리학자들은 빛의 "입자-파동 이원론"에 대해 이야기하기 시작했습니다. 빛이 전자기파라는 지식이 과학이 빛에 대해 아는 전부는 아님이 밝혀졌습니다. 과학자들은 빛에서 매우 흥미로운 특징을 발견했습니다.
어쨌든 빛은 어떻게든 입자 흐름의 행동으로 나타납니다.빛이 전달하는 에너지는 특수한 탐지기로 일정 시간 동안 세어본 결과 어쨌든 개별(전체) 조각으로 구성되어 있음이 밝혀졌습니다.
따라서 빛의 에너지는 개별 입자, 즉 "양자", 즉 에너지의 가장 작은 전체 부분으로 구성되어 있기 때문에 이산적이라는 것이 사실이 되었습니다. 에너지 단위(또는 양자)를 운반하는 이러한 빛 입자를 광자라고 부르게 되었습니다.
하나의 광자 에너지는 다음 공식으로 구합니다.
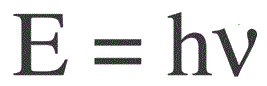
E — 광자 에너지, h — 플랑크 상수, v — 주파수.
독일의 물리학자 막스 플랑크는 처음으로 광파의 불연속성에 대한 사실을 실험적으로 확립하고 개별 광자의 에너지를 구하는 공식에 나타나는 상수 h의 값을 계산했습니다. 이 값은 6.626 * 10-34 J * s로 밝혀졌습니다. 플랑크는 1900년대 후반에 그의 작업 결과를 발표했습니다.

예를 들어 보라색 광선을 생각해 보십시오. 그러한 빛의 진동수(f 또는 v)는 7.5 * 1014Hz이고 플랑크 상수(h)는 6.626 * 10-34 J * s입니다. 이것은 보라색의 특징인 광자 에너지(E)가 5 * 10-19 J라는 것을 의미합니다. 이것은 매우 작은 에너지 부분이므로 포착하기가 매우 어렵습니다.
계류를 상상해보십시오. 하나의 단위로 흐르고 육안으로는 계류가 실제로 개별 물 분자로 구성되어 있음을 볼 수 없습니다. 그러나 오늘날 우리는 거시적인 물체인 흐름이 실제로는 개별적이라는 것을 알고 있습니다. 즉, 개별 분자로 구성되어 있습니다.
즉, 스트림이 흐를 때 통과하는 물 분자 수를 계산하기 위해 스트림 옆에 분자 계수기를 배치할 수 있다면 감지기는 항상 물 분자의 일부가 아닌 전체 수만 계산합니다.
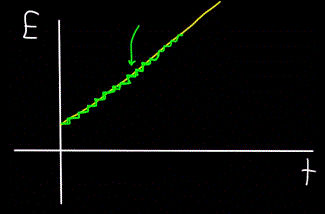
마찬가지로, 시간 t에서 계산된 광자 E의 총 에너지 그래프는 항상 선형(노란색 그림)이 아니라 단계적(녹색 그림)으로 나타납니다.
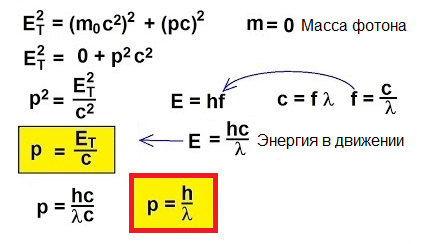
따라서 광자는 움직이고 에너지를 운반하므로 운동량이 있습니다. 그러나 광자는 질량이 없습니다. 그러면 어떻게 모멘텀을 찾을 수 있습니까?
사실, 빛의 속도에 가까운 속도로 움직이는 물체의 경우 고전 공식 p = mv는 간단히 적용할 수 없습니다. 이 특이한 경우에서 운동량을 찾는 방법을 이해하기 위해 특수 상대성 이론을 살펴보겠습니다.
1905년 알버트 아인슈타인은 이러한 관점에서 설명했습니다. 광전 효과... 우리는 금속판 안에 전자가 있고, 그 안에 전자가 양전하를 띤 원자핵에 이끌려 금속에 유지된다는 것을 알고 있습니다. 그러나 특정 주파수의 빛으로 그러한 판을 비추면 전자를 판에서 떨어뜨릴 수 있습니다.
마치 빛이 운동량을 가진 입자의 흐름처럼 행동하는 것과 같습니다 광자는 질량이 없지만 여전히 금속의 전자와 상호 작용하고 특정 조건에서 광자는 전자를 제거할 수 있습니다.
따라서 판에 입사하는 광자가 충분한 에너지를 가지면 전자는 금속에서 떨어져 나와 속도 v로 판 밖으로 이동합니다. 이렇게 녹아웃된 전자를 광전자라고 합니다.
녹아웃된 전자는 알려진 질량 m을 가지므로 특정 운동 에너지 mv를 갖게 됩니다.
광자의 에너지는 금속에 작용할 때 금속에서 전자가 빠져나가는 에너지(일함수)와 녹아웃된 전자가 움직이기 시작하는 전자의 운동 에너지로 변환됩니다. 금속 밖으로, 그것을 떠나.
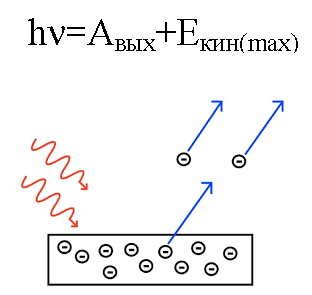
알려진 파장의 광자가 (금속에서 나온 전자의) 일 함수가 알려진 금속의 표면을 때린다고 가정합니다. 이 경우 주어진 금속에서 방출되는 전자의 운동 에너지와 속도를 쉽게 찾을 수 있습니다.
광자의 에너지가 전자가 일함수를 수행하기에 충분하지 않으면 전자는 단순히 주어진 금속의 표면을 떠날 수 없으며 광전자는 형성되지 않습니다.
1924년 프랑스 물리학자 루이 드 브로이 이에 따라 획기적인 아이디어를 제시 빛의 광자뿐만 아니라 전자 자체도 파동처럼 행동할 수 있습니다. 과학자는 심지어 전자의 가상 파장에 대한 공식을 유도했습니다. 이 파도는 나중에 "de Broglie 파도"라고 불 렸습니다.
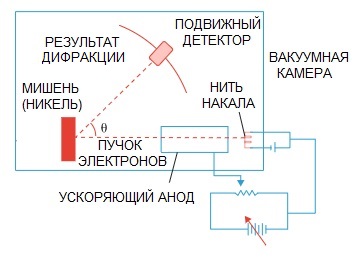
De Broglie의 가설은 나중에 확인되었습니다. 1927년 미국 과학자 클린턴 데이비슨과 레스터 저머가 실시한 전자 회절에 관한 물리 실험에서 마침내 전자의 파동성을 밝혀냈다.
전자 빔이 특수한 원자 구조를 통과했을 때, 검출기는 전자가 입자라면 논리적으로 예상되는 입자가 차례로 날아가는 것으로 사진을 기록했어야 하는 것 같습니다.
그러나 실제로는 파동 회절의 그림 특성이 있습니다. 게다가 이 파동의 길이는 de Broglie가 제안한 개념과 완전히 일치합니다.
궁극적으로 드 브로이의 아이디어는 보어의 원자 모형의 원리를 설명할 수 있게 했고, 나중에는 에르빈 슈뢰딩거가 이러한 아이디어를 일반화하고 현대 양자물리학의 토대를 마련하는 것을 가능하게 했습니다.
