패러데이의 전기 분해 법칙
패러데이의 전기분해 법칙은 마이클 패러데이가 1836년에 발표한 전기화학 연구에 기초한 정량적 관계입니다.
이 법은 방출된 물질의 양 사이의 관계를 결정합니다. 전기 분해 중 그리고 전해질을 통과한 전기의 양. 패러데이의 법칙은 두 가지입니다. 과학 문헌과 교과서에는 이러한 법칙에 대한 다양한 공식이 있습니다.
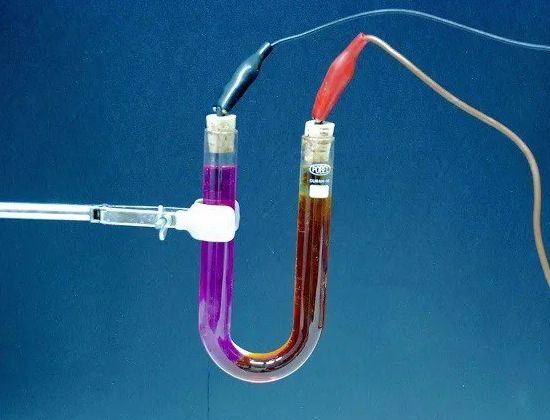
전기분해 - 통과하는 동안 구성 물질의 전해질로부터의 방출 전기... 예를 들어 전류가 약간 산성화된 물을 통과하면 물은 구성 요소인 가스(산소와 수소)로 분해됩니다.
전해질에서 방출되는 물질의 양은 전해질을 통과하는 전기의 양, 즉 전류의 강도와 이 전류가 흐르는 시간의 곱에 비례합니다. 따라서 전기분해 현상은 전류의 강도를 측정하고 결정하는 역할을 할 수 있습니다. 현재 단위.
전해질 - 용액 및 일반적으로 전류를 전도하는 복잡한 액체.배터리에서 전해질은 황산 용액(납) 또는 가성 칼륨 또는 가성 소다 용액(철-니켈)입니다. 갈바니 전지에서 모든 화합물(암모니아, 황산구리 등)의 용액도 전해질 역할을 합니다.
마이클 패러데이(1791~1867)
마이클 패러데이 (1791 — 1867) — 영국의 물리학자, 현대 전자기 현상 이론의 창시자. 그는 제본 작업장에서 견습생으로 직장 생활을 시작했습니다. 그는 초등 교육 만 받았지만 독립적으로 과학을 공부하고 화학자 Devi의 실험실 조교로 일했으며 위대한 실험 물리학 자 중 한 명인 위대한 과학자가되었습니다.
패러데이가 열렸습니다 전자기 유도 현상, 전기 분해의 법칙, 전기장 및 자기장의 교리를 개발하고 배치 현대 전자기장 개념의 기초… 그는 전자기 현상의 진동, 파동 특성에 대한 아이디어를 가진 최초의 과학자였습니다.
패러데이의 첫 번째 전기분해 법칙
전기분해 동안 전극에 침전되는 물질의 질량은 해당 전극으로 전달되는(전해액을 통과하는) 전기량에 정비례합니다. 전기량은 일반적으로 펜던트에서 측정되는 전기량을 나타냅니다.
패러데이의 전기분해 제2법칙
주어진 양의 전기(전하)에 대해 전기 분해 중에 전극에 증착되는 화학 원소의 질량은 해당 원소의 등가 질량에 정비례합니다. 물질의 등가 질량은 물질이 관련된 화학 반응에 따라 몰 질량을 정수로 나눈 값입니다.
또는
같은 양의 전기가 전기 분해 중에 전극에 서로 다른 물질의 등가 질량을 방출합니다. 어떤 물질의 당량 1몰을 방출하려면 같은 양의 전기, 즉 96485C를 소비해야 합니다. 이 전기화학 상수를 패러데이 수.
수학적 형태의 패러데이 법칙
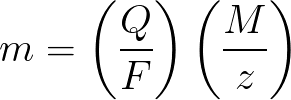
-
m은 전극에 증착된 물질의 질량입니다.
-
Q는 전기 분해 중에 전달된 펜던트의 총 전하 값입니다.
-
F = 96485.33 (83) C / mol — 패러데이 수;
-
M은 원소의 몰 질량(g/mol)입니다.
-
z - 물질 이온의 원자가 수(이온당 전자)
-
M / z — 전극에 적용된 물질의 등가 질량.
Faraday의 전기분해 제1법칙에 적용하면 M, F, z는 상수이므로 Q가 많을수록 m도 많아집니다.
Faraday의 전기분해 제2법칙에 따르면 Q, F, z는 상수이므로 M/z가 많을수록 m이 커집니다.
직류의 경우 우리는
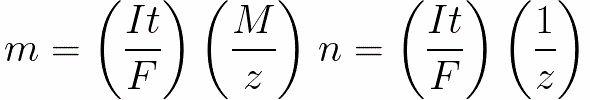
-
n은 전극에서 방출되는 몰수(물질의 양)입니다: n = m/M.
-
t는 전해질을 통해 직류가 통과하는 시간입니다. 교류의 경우 시간이 지남에 따라 총 전하가 합산됩니다.
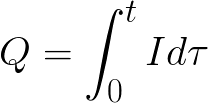
-
t는 총 전기분해 시간입니다.
패러데이의 법칙을 적용한 예
불활성 양극으로 황산나트륨 수용액을 전기분해하는 동안 음극과 양극에서 전기화학적 공정 방정식을 작성할 필요가 있습니다. 문제에 대한 해결책은 다음과 같습니다. 용액에서 황산나트륨은 다음 반응식에 따라 해리됩니다.
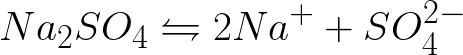
이 시스템의 표준 전극 전위는 다음과 같습니다.
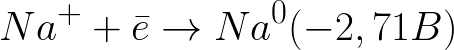
이것은 중성 매질(-0.41V)의 수소 전극보다 훨씬 더 음의 전위 수준입니다. 따라서 음극(음극)에서 물의 전기화학적 해리는 다음 계획에 따라 수소 및 수산화물 이온의 방출로 시작됩니다.
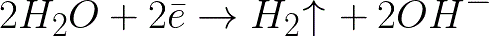
그리고 음으로 하전된 음극에 접근하는 양으로 하전된 나트륨 이온은 용액의 인접한 부분에서 음극 근처에 축적될 것입니다.
양극(양극)에서 물의 전기화학적 산화가 발생하여 다음과 같은 방식으로 산소가 방출됩니다.
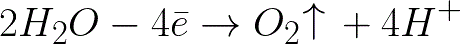
이 시스템에서 표준 전극 전위는 +1.23V이며 이는 다음 시스템에서 발견되는 표준 전극 전위보다 훨씬 낮습니다.
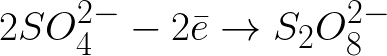
양전하를 띤 양극으로 이동하는 음전하를 띤 황산 이온은 양극 근처의 공간에 축적됩니다.

