전류원
전류—그것을 만들고 유지하는 방법
 하전 입자의 규칙적인 운동을 전류라고 합니다. 전선에 전류를 흐르게 하려면 전선에 전기장을 만들어야 합니다. 대전체가 전선으로 접지에 연결되면 전선에 단기 전류가 발생합니다. 전선에서 전기장을 얻고 유지하려면 전류원을 사용하십시오.
하전 입자의 규칙적인 운동을 전류라고 합니다. 전선에 전류를 흐르게 하려면 전선에 전기장을 만들어야 합니다. 대전체가 전선으로 접지에 연결되면 전선에 단기 전류가 발생합니다. 전선에서 전기장을 얻고 유지하려면 전류원을 사용하십시오.
모든 전류원에서 양전하 입자와 음전하 입자를 분리하는 작업이 수행됩니다. 분리된 입자는 소스의 극점에 축적됩니다. 극 사이에 전기장이 생성됩니다. 전선으로 연결하면 전선에서 필드가 발생합니다.
전기 기계에서 전하의 분리는 기계적 에너지의 도움으로 이루어집니다. 동시에 그것은 전기가 된다. 열전대에서 내부 에너지는 전기 에너지로 변환됩니다. 핵 배터리는 원자 에너지를 전기로 변환합니다.
광전지는 빛 에너지를 전기 에너지로 변환합니다. 태양 전지는 광전지로 구성됩니다.빛 에너지를 가장 쉽게 이용할 수 있는 곳에서 사용됩니다.
강, 석탄, 석유 및 원자의 에너지는 발전소에서 전기 에너지로 변환됩니다. 전류의 가장 일반적인 소스는 갈바니 전지와 배터리입니다.
갈바니 전지
갈바니 전지는 화학 에너지가 전기 에너지로 변환되는 전류원입니다.
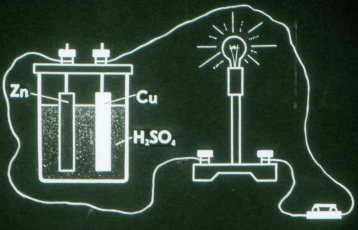
이것이 가장 단순한 갈바닉 전지가 작동하는 방식입니다.
최초의 전기화학 전지는 1799년 볼트에 의해 발명되었습니다. 개별 요소로부터 그는 "볼트 극"이라고 하는 배터리를 구성했습니다. 갈바니 전지에서 전극은 반드시 서로 다른 방식으로 용액과 상호 작용해야 하며, 이것이 전극이 서로 다른 재료로 만들어지는 이유입니다.

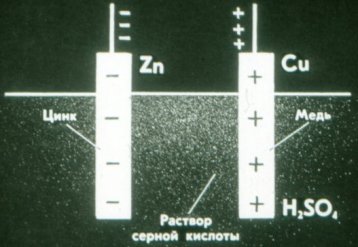
Volta 전지의 아연판은 음전하를 띠고 구리판은 양전하를 띤다.
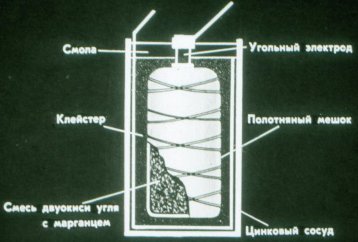
이것이 건식 갈바닉 전지가 작동하는 방식입니다. 액체 대신 두꺼운 페이스트를 사용합니다.
배터리는 여러 요소로 구성될 수 있습니다.

전기 램프의 전구와 기타 다양한 휴대용 전기 제품 및 어린이 장난감은 갈바니 전지로 전원을 공급받습니다. 갈바니 전지의 전극이 모두 소모되면 전지가 새 것으로 교체됩니다.
배터리
배터리는 전극이 소모되지 않는 화학적 전류원입니다. 가장 간단한 배터리는 황산 용액에 담긴 두 개의 납판으로 구성됩니다.
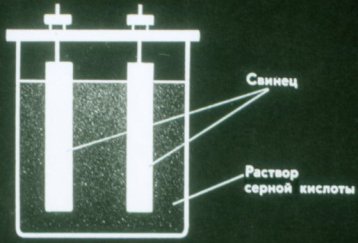
이러한 배터리는 여전히 전류를 공급하지 않습니다. 사용하기 전에 충전해야 합니다. 이렇게 하려면 배터리의 극을 각 전류 소스의 동일한 극에 연결하십시오.
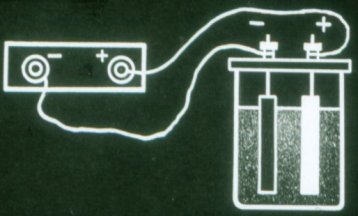
충전하는 동안 배터리를 통해 흐르는 전류는 플레이트의 화학적 구성을 변경합니다. 배터리의 화학 에너지가 증가합니다.
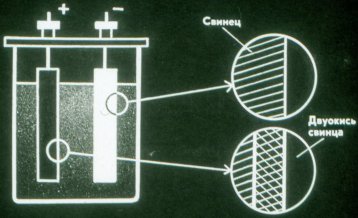
배터리가 방전되면 화학 에너지를 전기 에너지로 변환합니다. 방전된 배터리를 충전할 수 있습니다.
배터리는 별도의 배터리에서 수집됩니다.
산성(납) 배터리 외에도 알카라인(철-니켈) 배터리가 사용됩니다.
니켈 철 배터리:
니켈-카드뮴 및 니켈-금속 수소화물 배터리도 오늘날 널리 사용됩니다. 은-아연 배터리는 항공 및 우주 분야에서 사용되며 새로운 유형의 배터리: 리튬 이온, 리튬 폴리머는 휴대폰, 태블릿 및 기타 최신 휴대용 장비에 사용됩니다.
배터리는 전류 소스가 새 것으로 교체하는 것보다 재충전하는 것이 더 유리한 경우에 사용됩니다. 자동차에서 배터리는 엔진을 시동하고 다양한 장치를 작동하는 데 사용됩니다. 우주에서 배터리는 태양 전지판으로 충전됩니다. 방전되면 무선 송신기 및 장비에 전원을 공급합니다.
또한보십시오: 배터리. 계산 예

